Description du projet
Source de nombreuses études, trésor des côtes méditerranéennes, la posidonie est l’objet de toutes les curiosités. Dans une série de 3 volets, nous explorerons les divers aspects de son écologie, de sa biologie, ses services pour l’Homme, les menaces qui pèsent sur elles, ainsi que les solutions pour la protéger.
Texte par Jean-Vincent Vieux-Ingrassia – NaturDive
Menaces pour sa survie
L’ensemble des services écosystémiques rendu par les herbiers à P. oceanica rend son déclin particulièrement préoccupant, déclin qui est dû à sa destruction et favorisé par des facteurs dits ‘de stress’. Ces facteurs de stress comprennent les aménagements intensifs des côtes, la pollution, les espèces exotiques envahissantes, les pratiques de pêche non durables, le tourisme mal planifié (Montefalcone et al., 2009; Coll et al., 2012; Katsanevakis et al., 2014; Randone et al., 2017; Houngnandan 2020), et les autres causes du changement climatique, tel que l’acidification des océans (Martin et al., 2014; Gaylord et al., 2015; Zunino et al., 2017; Houngnandan 2020). D’un point de vue naturel, les évènements météorologiques et tectoniques exceptionnels ainsi que les maladies ne sont pas à oublier pour expliquer les processus de régression des herbiers (Duarte et al., 2012; Pergent et al., 2014; Houngnandan 2020).
On peut donc établir deux grandes catégories de menaces : les impacts liés à l’Homme dits anthropiques, et les impacts naturels.
L’un des impacts anthropiques les plus fréquents est l’action mécanique directe des ancres de bateaux. Celles-ci arrachent les pousses de P. oceanica, ou des sections de matte, favorisant la formation d’espaces importants au sein de l’herbier, on appelle ceci des intermattes. L’une des premières conséquences est l’augmentation de l’érosion des sols, favorisée par l’hydrodynamisme, ce qui fragmente la prairie (Pasqualini et al., 2000; Houngnandan 2020). Cet impact est spectaculaire dans le cas des ancres de paquebots et navires de guerre qui provoquent un labour très important du fond marin, et arrachent les rhizomes en grande quantité (Houngnandan 2020). On peut remarquer de fortes conséquences négatives sur les herbiers situés dans des baies abritées, car c’est un lieu habituel de mouillage pour les bateaux de plaisance.
En exemple, au mouillage, sous l’effet de la houle et du vent, les bateaux bougent et peuvent faire un tour complet. Les ancres, pouvant peser plus de 500 kg pour les gros yachts, et les chaînes, balayant et ratissant irrémédiablement les fonds, entraînent des dommages physiques sur ces prairies subaquatiques jusqu’à détruire, en une nuit, 2.000 m² d’herbiers.
Mais, dans un second temps, la fragmentation des prairies, due à l’impact des mouillages, et particulièrement ceux des gros bateaux, favorise les invasions et les implantations d’espèces non-indigènes, comme l’algue Caulerpa taxifolia (Occhipinti-Ambrogi 2007; Houngnandan 2020). Celle-ci, non contente de prendre la place laissée vacante par les arrachages sauvages, va également profondément altérer la repousse des prairies, même après sa forte régression (Molenaar et al., 2009). La posidonie a beaucoup de mal à revenir à son état initial.
Globalement, selon le niveau d’impact, les trous dans l’herbier peuvent ‘cicatriser’ si les fonctions vitales sont optimales et si l’impact n’est pas répétitif. A contrario, si l’ancrage persiste, l’herbier se dirigera vers un morcellement et une destruction de la matte souterraine, créant une cascade de conséquences néfastes pour les écosystèmes côtiers.
À noter que le modèle d’ancre est également important. En effet, l’ampleur des dommages infligées à P. oceanica dépend du type d’ancrage adopté lors du processus de mouillage (Milazzo et al., 2004). Une ancre à grappin pliant, une ancre de type « Hall » ou une ancre « Danforth » n’auront pas le même impact. En comparaison des deux autres, l’ancre « Hall » semble être préférable pour minimiser le contrecoup de l’ancrage sur les herbiers de posidonie (Milazzo et al. 2004).
En ce qui concerne l’artificialisation des côtes, trois points sont à retenir. Tout d’abord, les herbiers sont sensibles à la turbidité de l’eau, c’est-à-dire son opacité, si l’eau est plus ou moins claire. Les travaux en bordure de côte déclenchent une hyper-sédimentation du substrat ; le sable et les sédiments en surplus étouffent les rhizomes et modifient la qualité des sols. Deuxièmement, cette opacité va réduire drastiquement la luminosité ambiante et empêcher donc une photosynthèse de qualité. Enfin, les constructions côtières peuvent modifier l’hydrodynamisme local et donc éroder la matte voire provoquer un ensevelissement total de l’herbier (Pérez et al., 2008; Houngnandan 2020).
Herbier de posidonie situé proche du débarcadère de l’île Sainte-Marguerite © Jean-Vincent Vieux-Ingrassia
Le ré-ensablement des plages affecte également les herbiers de posidonie. À court terme, après ajout rapide de sédiments, des symptômes d’alertes ont été détectés comme la réduction de la taille des pousses, des changements d’espèces vivant accrochées aux feuilles ou encore l’épuisement des stocks d’amidon de la plante (González-Correa et al., 2009). A long terme, on assiste à une pression durable sur la plante, en ce qui concerne les caractéristiques des sédiments, ce qui ralentit sa récupération naturelle après perturbation. Des périodes d’enfouissements plus longues encore provoquent la mort de la plante et déséquilibre le profil de la plage, provoquant un recul plus important du rivage (González-Correa et al., 2008; Aragonès et al., 2015).
Un autre impact altère la chimie de l’eau et du substrat, à tel point que les herbiers peuvent montrer une mortalité très importante : ce sont les fermes aquacoles (Ruiz et al., 2001; Holmer et al., 2003; Frederiksen et al., 2007; Díaz-Almela et al., 2008; Pérez et al., 2008; Holmer et al., 2009; Kletou et al., 2018). Depuis plusieurs années, la demande en poissons et fruits de mer des populations ne cesse d’augmenter. En 20 ans, il y a eu une croissance spectaculaire de la production aquacole méditerranéenne, s’accroissant d’environ 5 % par année (Massa et al., 2017).
Les excréments des poissons, ainsi que la nourriture donnée en excès, libèrent une importante quantité de matière organique dans l’eau, ce qui conduit à une explosion des algues poussant sur les feuilles des posidonies, empêchant une bonne photosynthèse car prenant la place de la plante, donc entrant en compétition avec elle (Pérez et al., 2008; Holmer et al., 2009). En conséquence, les phytophages vont avoir un impact d’herbivorie plus important sur l’herbier (Holmer et al., 2003; 2009). Ce n’est pas tout, car les rejets des fermes aquacoles amènent également des sulfures dans les racines et surcharge les sédiments en matière organique (Frederiksen et al., 2007; Díaz-Almela et al., 2008; Pérez et al., 2008). Cet enrichissement organique mène donc à des conditions benthiques, c’est-à-dire du fond marin, toxiques et anoxiques (Pérez et al., 2008; Kletou et al., 2018). Enfin, les cages elles-mêmes font de l’ombre aux herbiers et diminuent la luminosité disponible (Ruiz et al., 2001). Les herbiers marins exposés aux fermes piscicoles ont donc les taux de recrutement les plus bas, limités à une multiplication végétative et une croissance horizontale dans des conditions de faible luminosité (Kletou et al., 2018).
Récemment, il a été mis en évidence que les rhizomes de la posidonie accumulent des composés de crèmes solaires, notamment des parabènes (Agawin et al., 2022). Chez les producteurs primaires, tel que la posidonie, ces composés sont souvent associés avec une diminution de la production de pigments photosynthétiques, une inhibition de la croissance cellulaire, des dommages sur les structures internes, des altérations morphologiques cellulaires ou encore une atteinte à l’activité métabolique (Agawin et al., 2022).
Néanmoins, de récentes études ont également mis en évidence que l’élévation de la température de la mer, provoquée par les changements climatiques globaux, était l’une des principales explications du déclin global des herbiers, particulièrement ceux de P. oceanica (Marbà & Duarte 2010; Pergent et al., 2014; Houngnandan 2020). En effet, la posidonie perdure dans des eaux entre 13 et 28°C. On peut donc facilement imaginer les conséquences d’une eau plus chaude sur la physiologie de cette plante fragile.
Il se trouve que l’augmentation de la température affecterait également un consommateur de la posidonie : la saupe. Des expériences ont montré que l’impact d’herbivorie de ce poisson augmente significativement avec la température, et il cible plus souvent la posidonie. Conjointement à cela, les herbiers présentent une croissance réduite à mesure que l’eau devient plus chaude. Même si on ne sait pas si la posidonie peut supporter une telle intensification de broutage, cela s’ajoute à la longue liste des pressions dont elle est déjà confrontée (Bunuel et al., 2020).
Les vagues de chaleur (> 29°C) prédites par le réchauffement de la Méditerranée, couplées au surpâturage des saupes et à un enfouissement grandissant des semis, compromettent la croissance et l’activité photosynthétique de la posidonie. On s’attend à des conséquences négatives dépendantes de la profondeur, ce qui amène l’idée que les herbiers les plus proches de la surface seront les premiers affectés. La reproduction sexuée, par les fruits, s’en trouverait aussi fortement impactée, ce qui poserait un problème de diversité génétique à long-terme et de dispersion de l’espèce dans l’espace (Guerrero-Meseguer et al., 2020).
Même si presque aucun herbier n’échappe aux impacts physiques des activités humaines, ceux-ci sont renforcés par les conditions environnementales changeantes et pèsent lourd sur l’état de conservation de cette espèce. L’accumulation des facteurs de stress affecte donc négativement les herbiers de posidonies, surtout au niveau urbain, sa décadence étant liée à 67,6 % aux activités physiques anthropiques (Marbà et al., 2014).
Les dernières données disponibles, sur des zones ayant des informations de distribution historique de l’espèce, estiment qu’entre 13 % et 50 % des herbiers marins semblent avoir été perdus au cours des 50 dernières années, et que les restants pourraient encore s’amoindrir de 50 % au cours des 20 prochaines années pour devenir plus fragmenté encore (Marbà et al., 2014; Telesca et al., 2015; Houngnandan 2020). Les anciennes prairies de P. oceanica déclinent donc à un rythme de plusieurs centaines de fois plus rapide que la vitesse à laquelle elles se propagent lors de leur formation. Une situation dont cette espèce à croissance lente et à longue durée de vie n’est pas capable de se remettre (Marbà et al., 2014; Telesca et al., 2015; Houngnandan 2020).
Evolution de l’étendue des herbiers de posidonie entre les Iles de Lérins et à la Pointe Croisette de Cannes – photos de 1950 et 2004
Les Solutions
Toutes ces menaces pèsent lourd sur les épaules de la posidonie, c’est pourquoi de nombreux chercheurs se sont penchés sur des techniques de restauration et de protection de cette espèce. L’Union Internationale pour la Conservation de la Nature (UICN) classe la posidonie dans sa liste rouge des espèces en danger, sa population étant en régression inquiétante. C’est pourquoi de nombreuses mesures juridiques sont prises afin de la protéger.
Petit rappel de la réglementation :
1. Au niveau méditerranéen, la posidonie est inscrite à l’annexe II de la Convention de Barcelone (liste des espèces en danger ou menacées). L’espèce est également inscrite à l’annexe I (Espèces de flore strictement protégées) de la Convention de Berne.
2. Au niveau européen par la directive européenne « habitat, faune, flore ». De plus, les règlements de pêche de l’UE limitent les activités de chalutage à proximité du rivage (soit au dessus de 50m, soit à une certaine distance de la côte), ce qui constitue une mesure de protection indirecte pour l’espèce.
3. En France, la protection juridique de la posidonie relève de la loi du 10 juillet 1976, relative à la protection de la nature, et de son décret d’application du 25 novembre 1977, relatif à la protection de la faune et de la flore sauvages du patrimoine naturel français. À cela s’ajoute, l’arrêté du 19 juillet 1988 et le décret du 20 septembre 1989 de la Loi littorale. Ce décret d’application impose notamment la réalisation d’une notice d’impact spécifique sur le milieu marin, et en particulier sur l’herbier de Posidonie, pour tout projet d’aménagement littoral. De plus, la présence d’herbiers doit également être prise en compte dans les dossiers d’aménagement et les études d’impact.
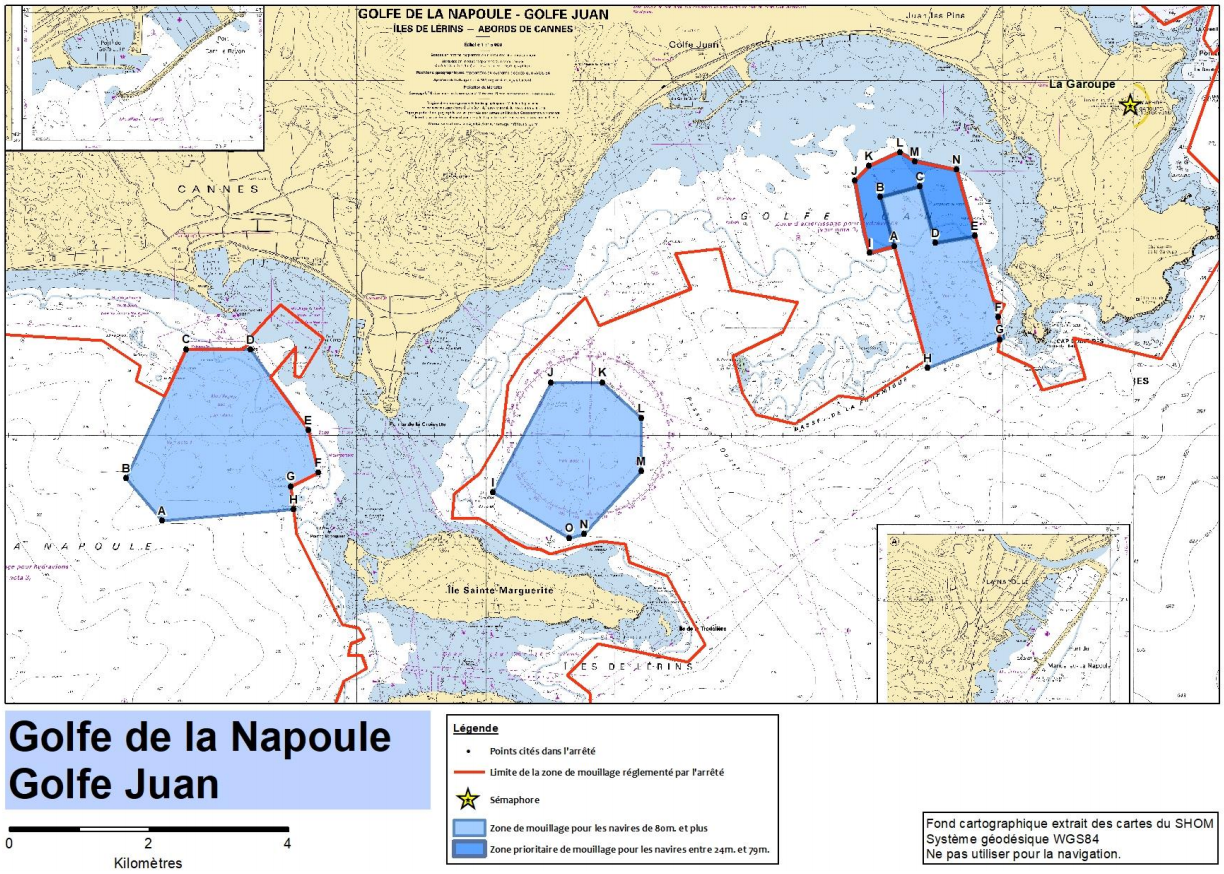
Le 12 octobre 2020, le préfet maritime de la Méditerranée a signé des arrêtés réglementant le mouillage des navires de plus de 24 mètres – voir via ce lien : naturdive.com/yachting. Ces arrêtés identifient des zones d’interdiction au mouillage, notamment des zones hébergeant des herbiers de posidonie. Ces unités n’ont donc plus le droit de mouiller dans ces zones précises ! Ceci va dans le sens des études d’impact qui pointent les effets spectaculaires des ancres des yachts sur cette espèce.
En parallèle, organiser le mouillage sur le littoral, particulièrement fréquenté pendant l’été, va permettre de décongestionner des zones côtières entières, jusqu’alors propices aux conflits d’usage et aux accidents (Martin et al., 2018).
La première solution est donc de limiter les dégâts anthropiques déjà présents car l’urbanisation et la densité des populations côtières sont les deux pressions anthropiques les plus reliées au déclin de la posidonie (González-Correa et al., 2007; Montefalcone et al., 2009; Houngnandan et al., 2020). Il faudrait donc stopper l’urbanisation mais aussi limiter les zones d’ancrages, diminuer l’aquaculture – voir l’article « Menaces pour sa survie ».
En exemple, la régression massive, de l’ordre de 44 %, des prairies de posidonie près de Marseille a été liée aux eaux usées déversées pendant 12 ans (Pergent-Martini 1994) ; la construction de deux ports, dans la région d’Alicante, abritant 1404 petits et moyens bateaux ont provoqué la destruction d’au moins 11 hectares de prairie et la dégradation de 14 autres hectares (Fernández Torquemada et al., 2005) ou encore les 11,2 hectares perdus et 9,8 autres considérablement dégradés par l’aquaculture pendant 10 ans dans le sud-est de l’Espagne, dans la baie d’Hornillo à Aguilas.
Un arrêt, ou a minima une importante atténuation, de ces pratiques est déjà un point important pour la conservation de cette espèce indispensable.
La deuxième solution est de protéger officiellement des zones entières de toutes pressions anthropiques, c’est-à-dire augmenter le nombre et la surface des Aires Marines Protégées (AMP) et des Autres Mesures Spatiales de Conservation (AMSC). En 2022, le nombre d’AMPs, et d’AMSCs, est de 1231, toutes désignations confondues, représentant 7,14 % de la Méditerranée, soit 179 798 km2. De nombreuses zones ont pour objectif de préserver la posidonie. En effet, 39,77% des herbiers de posidonie de la Méditerranée sont couverts par des AMPs et AMSCs. Pour être plus précis, les limites extracôtières de ces zones sont généralement déterminées par les limites des herbiers locaux et de leur extension en profondeur (Francour et al., 2001; Montefalcone et al., 2009). D’ailleurs, dans ces zones, on ne remarque pas de déclin de la posidonie comme on pourrait le constater en dehors, au contraire la dynamique de la population est positive avec d’exceptionnelles croissances végétatives dans certaines zones comme autour de l’île de Zembra, en Tunisie (González-Correa et al., 2007; Montefalcone et al., 2009).
Néanmoins, la simple protection officielle ne suffit pas si la gestion est inexistante (Allison et al., 1998 ; Montefalcone et al., 2009). En effet, il a été montré que des prairies de zones protégées et celles de zones modérément anthropisées, mais à fort trafic touristique, avaient des états de santé similaires. Ce qui suggère que la protection juridique et les restrictions officielles ne sont pas suffisantes pour assurer une préservation optimale des herbiers (Montefalcone et al., 2009).
Des sources extérieures ont donc de plus grands effets sur la biodiversité des AMPs que les activités au sein de celles-ci. Il est donc évident qu’un plan de gestion à grande échelle est fondamental, et doit s’étendre au-delà des AMPs prises individuellement (Allison et al., 1998 ; Montefalcone et al., 2009).
La troisième solution est la restauration des herbiers endommagés. Plusieurs techniques existent et montrent des efficacités variables. La difficulté globale est d’arriver à fixer les boutures dans le sédiment mais également à concevoir des structures d’appuis capable de résister aux vagues ou à l’action des courants de fonds.
Tout d’abord, des recherches ont suggéré l’utilisation de fragments de posidonie issus de tempête (Molenaar & Meinesz 1995; Vangeluwe et al., 2004; Balestri et al., 2010; Ward et al., 2020). En effet, durant les tempêtes hivernales, de nombreux fragments, c’est-à-dire des rhizomes rampants ou dressés, s’échouent sur les plages et forment des banquettes. L’objectif est de les récupérer, avant qu’ils ne se dessèchent, et de les replanter. Les avantages sont multiples puisqu’il a été démontré que 50 % des implants, après la première année, étaient toujours présents et ont même développé de nouvelles pousses, que l’effort de récolte, sur les rivages, est faible et que la posidonie déjà existante n’est pas impactée par ce processus de restauration (Molenaar & Meinesz 1995; Vangeluwe et al., 2004; Balestri et al., 2010; Ward et al., 2020; Piazzi et al., 2021). Donc de grands avantages avec de très faibles inconvénients.
L’une des techniques sous-marines est de planter les fragments à 5 cm l’un de l’autre en quatre rangées de six fragments sur six grilles de 25 * 15 cm (Molenaar & Meinesz 1995). Les rhizomes rampants sont placés de préférence à l’extérieur des grilles, pour reproduire leur positionnement dans les herbiers naturels (Ward et al., 2020).
Deux méthodes de transplantation ont été récemment testées, basées sur la technique des grilles expliquée ci-dessus :
1) Planter les fragments, espacés de 5cm, sur 2cm de profondeur puis les maintenir avec des pousses de bambou, positionnés de chaque côté du fragment, pour former un « V » inversé (Ward et al., 2020).
2) Enlever 5cm de sédiments et placer un grand plateau composés de pots de fleurs en fibre de coco autour de la grille de fragments. Les pots ont été mis à l’envers et une incision a été faite entre chaque rangée de pots pour permettre aux rhizomes de pénétrer dans le sédiment en dessous. Les pots ont été recouverts de sédiments pour laisser le rhizome partiellement enterré avec les pousses émergentes (Ward et al., 2020).
A et D : Les fragments issus de tempêtes sont plantés en quatre rangées de six pour former des grilles de 15 x 25 cm pour les deux méthodes de replantation. B et C : des pousses de bambou sont insérées de part et d’autre du fragment pour former un « V » inversé. E et F : Les pots en fibre de coco sont inversés et recouverts de sédiments pour agir comme stabilisateur de sédiments © Ward et al., 2020.
Les résultats suggèrent que la technique des bambous fonctionnent mieux avec des rhizomes rampants tandis que les pots de coco donnent de meilleurs résultats avec des rhizomes dressés (Ward et al., 2020). Puisque l’on peut ramasser les deux types de rhizomes sur le rivage, une approche de transplantation mixte est recommandée (Ward et al., 2020). Néanmoins, beaucoup d’études privilégient l’utilisation des rhizomes rampants car leur taux de survie y est bien supérieur et ceux-ci colonisent mieux le substrat nu entourant les zones réimplantées (Molenaar & Meinesz 1995; Vangeluwe et al., 2004; Balestri et al., 2010; Ward et al., 2020).
A noter que la nature du substrat, où sont plantés les transplants, a une incidence fondamentale sur le taux de survie des fragments (Molenaar & Meinesz 1995; Terrados et al., 2013; Pirrotta et al., 2015; Ward et al., 2020), ainsi que la saison de transplantation et que l’espacement des pousses (Molenaar & Meinesz 1995; Vangeluwe et al., 2004; Ward et al., 2020; Piazzi et al., 2021). En effet, la transplantation sur de la matte morte fournit les meilleurs résultats car la présence de matte morte indique que les conditions environnementales du passé ont permis la croissance de la posidonie et représente donc le meilleur site de plantation (Molenaar & Meinesz 1995; Terrados et al., 2013; Pirrotta et al., 2015; Ward et al., 2020). La matte morte permet la plantation des fragments sans ancrage artificiel ce qui facilite les travaux de restauration sans compromettre la survie des semis (Molenaar & Meinesz 1995; Terrados et al., 2013; Pirrotta et al., 2015; Ward et al., 2020).
Cette technique pourrait être réalisée conjointement avec la création de zones sans ancrages ou la mise à disposition de bouées fixes afin d’optimiser la régénération des herbiers endommagés (Ward et al., 2020).
Certains chercheurs se sont également penchés sur l’adaptation des techniques de bouturage terrestre au milieu marin, en utilisant les fragments issus de tempête (Cinelli et al., 2007; Piazzi et al., 2021). Les résultats préliminaires soulignent que les matériaux utilisés sont stables dans le temps, résistants aux conditions marines, simple à mettre en place et le coût est acceptable (Cinelli et al., 2007). Mais les matériaux n’étaient pas biodégradables dans la première étude.
Une étude, de 2021, a donc comparé ces mêmes matériaux avec leur penchant biodégradable, notamment des tapis constitués de mailles de noix de coco couplées à une double maille tissée en acier torsadé (Piazzi et al., 2021). Le maillage est de 8 * 10 cm pour une épaisseur de 5cm.
Résultats : l’utilisation de ces tapis dégradables fournissent une technique utile et rentable pour les projets de restauration à grande échelle car ils garantissent l’ancrage des fragments à la matte morte, par une auto-facilitation naturelle de la plante (Piazzi et al., 2021). En effet, le maillage imite l’action naturelle d’herbiers déjà établis en facilitant l’agrégation dense de racines et de rhizomes. De plus, ces structures, comparées aux autres techniques comme les grilles, les cadres en béton ou les bâtons métalliques, ont amélioré la sédimentation pour la stabilisation du fond et la colonisation d’autres organismes tels que des macro-algues et des invertébrés divers, contribuant ainsi à générer un habitat naturel (Piazzi et al., 2021).
Une autre approche est d’utiliser des fruits mûrs produits par des herbiers (Balestri et al., 1998; Terrados et al., 2013). La germination est réalisée en laboratoire pendant deux mois puis des plants de taille homogène sont sélectionnés afin d’être attachés à une grille de 25 * 25 cm via un fil de nylon et mis en mer (Balestri et al., 1998). Là encore, la nature du substrat se révèle être important car les semis placés sur de la matte morte ont montré un taux de survie plus élevée que ceux observés dans des conditions de laboratoire (Balestri et al., 1998). Cette technique peut être très utile car les fruits échoués sur les plages finiront par mourir donc pourquoi ne pas les utiliser pour comprendre les facteurs affectant le début de la vie de la posidonie et évaluer les techniques de plantation. Un autre avantage est génétique. Car l’utilisation de fragments végétatifs, donc des rhizomes, est lié à une faible diversité génétique (Williams 2001), et l’utilisation de fruits pourrait au contraire amener de la diversité afin d’éviter une homogénéité génétique synonyme de maladies et de réduction de l’efficacité de reproduction (Terrados et al., 2013).
Une autre idée est d’utiliser des récifs artificiels pour replanter de la posidonie arrachées par les tempêtes (Tomasello et al., 2019). Ces récifs artificiels, immergés à 13m de fond, sont en béton armé et composés d’une base de 2*3m avec des abris communicants, et d’une hauteur variant entre 1m et 1m80 (Tomasello et al., 2019). Les posidonies sont fixées par un procédé adapté aux substrat durs. Résultats : 70 % des transplants ont survécu, ce qui permet de penser que la posidonie peut développer des capacités adaptatives pour subsister sur des substrats durs (Tomasello et al., 2019). La posidonie pourrait également améliorer l’esthétique, parfois brute, des récifs artificiels.
Système d’ancrage pour la posidonie sur substrat dur et de la posidonie ‘plantée’ sur la structure artificielle © Tomasello et al., 2019
Pour finir, dans la région d’Alicante en Espagne, la transplantation d’un large herbier de 200m2 a été testée afin d’éviter ou d’atténuer sa destruction suite à l’expansion d’une marina (Sánchez-Lizaso et al., 2009). Malgré les techniques inédites mises en place et les plus de 100 jours de travaux, le déplacement de l’herbier a été suivi par une mortalité importante (~85%). Malgré tout, les pousses survivantes ont persisté dans le temps. Mais la quantité d’argent et de temps qui est nécessaire pour relocaliser ces dizaines d’hectares rend l’objectif de préservation intenable (Sánchez-Lizaso et al., 2009).
Une autre transplantation de ce type a été faite à Monaco en 2017 et a consisté au déplacement d’un herbier de 500m2 mais par une technique innovante d’élimination des mottes (Descamp et al., 2017). La posidonie a été retirée de son substrat par une bêche spécialement modifiée. Les piques coupent les racines et les rhizomes et forment une motte compacte allongée. Une fois la motte de posidonie enlevée, celle-ci est placée dans un panier suspendu à 10m de profondeur afin de la transporter jusqu’au site de replantation (Descamp et al., 2017). 37 % de l’herbier initial a ainsi été transplanté. Plusieurs mois plus tard, aucune nécrose ou mortalité n’a été détecté, et de jeunes feuilles ont été observées prouvant que le cycle de vie n’a pas été interrompu par cette technique de transplantation (Descamp et al., 2017). Un suivi est depuis réalisé. Pour être certains de l’efficacité de ces projets de restauration, des suivis d’au moins 6 ans devraient être mis en place (Pirrotta et al., 2015). Le premier suivi des transplants monégasque sur fonds sableux, après 3 années, a montré une stabilisation de la densité des pousses et une tendance de colonisation des rhizomes plagiotropes, horizontaux (Boudouresque et al., 2021).
Légende de la première photo : 1) Paniers de transports, 2) Pelleteuse à bras long, 3) Auto-élévatrice, 4) Herbier à transplanter, 5) Contrôle vidéo, 6) Cartographie par photogrammétrie et mise en place de cibles dans les herbiers avant prélèvement, 7) Visées laser, 8) Transplanteur, 9) Plate-forme mobile / L’autre photo montre le transplanteur en opération © Descamp et al. 2017
Malgré les résultats positifs de ces méthodes très variées, toutes ces solutions sont inutiles si l’agent de destruction n’est pas stoppé. Compte tenu des incertitudes et des contraintes liées à la restauration, la régulation des activités anthropiques qui endommagent les prairies reste la meilleure stratégie pour préserver cet écosystème côtier précieux et fragile (Terrados et al., 2013).
Merci à Samuel Jeglot, Ioana Stoicescu et Stéphane Jamme pour leurs contributions photographiques
Bibliographie
Publications scientifiques
– Agawin N. S. R., Sunyer-Caldù A., Diaz-Cruz M., Frank-Comas A., Garcia-Marquez M. G. & Tovar-Sanchez A. (2022) Mediterranean seagrass Posidonia oceanica accumulates sunscreen UV filters. Marine Pollution Bulletin, Vol 176, https://doi.org/10.1016/j.marpolbul.2022.113417.
– Allison G. W., Lubchenco J. & Carr M. H. (1998) Marine reserves are necessary but not sufficient for marine conservation. Ecological Application 8 (1), 79–92.
– Aragonès L., Garcia-Barba J., Garcia-Bleda E., Lopez I. & Serra J. C. (2015) Beach nourishment impact on Posidonia oceanica : Case study of Poniente Beach (Benidorm, Spain). Ocean Engineering, 107, 1-12.
– Arnaud-Haond S., Duarte C. M., Diaz-Almela E., Marbà N., Sintes T. & Serrao E. A. (2012) Implications of Extreme Life Span in Clonal Organisms: Millenary Clones in Meadows of the Threatened Seagrass Posidonia oceanica. PLoS ONE 7(2): e30454. doi:10.1371/journal.pone.0030454
– Badalamenti F., Alagna A. & Fici S. (2015) Evidences of adaptive traits to rocky substrates undermine paradigm of habitat preference of
the Mediterranean seagrass Posidonia oceanica. Sci. Rep. 5, 8804.
– Balestri E., Piazzi L. & Cinelli F. (1998) Survival and growth of transplanted and natural seedlings of Posidonia oceanica (L.) Delile in a damaged coastal area. J. Exp. Mar. Biol. Ecol, 228 : 209 –225.
– Balestri E., Vallerini F. & Lardicci C. (2010) Storm-generated fragments of the seagrass Posidonia oceanica from beach wrack –A potential source of transplants for restoration. Biological Conservation, 144, 1644-1654.
– Bonhomme D., Boudouresque C. F., Astruch P., Bonhomme J., Bonhomme P., Goujard A. & Thibaut T. (2015) Typology on the reef formations of the Mediterranean seagrass Posidonia oceanica, and the discovery of extensive reefs in the Gulf of Hyères (Provence, Mediterranean). Sci. Rep. Port-Cros natl. Park, 29 : 41-73.
– Borovec O. & Vohník M. (2018) Ontogenetic transition from specialized root hairs to specific root-fungus symbiosis in the dominant Mediterranean seagrass Posidonia oceanica. Scientific Report, 8 : 10773. DOI:10.1038/s41598-018-28989-4
– Boudouresque C. F. & Meinesz A. (1982) Découverte de l’herbier de Posidonie. Cahiers Parc National de Port-Cros 4, 79.
– Boudouresque C. & Jeudy de Grissac A. (1983) L’herbier à Posidonia oceanica en Méditerranée: les interactions entre la plante et le sédiment = Posidonia oceanica seabed in Mediterranean Sea; interactions between plant and sediments. J. Rech. Oceanographic 8, 99–122.
– Boudouresque C.F., Bernard G., Pergent G., Shili A. & Verlaque M. (2009) Regression of Mediterranean seagrasses caused by natural processes and anthropogenic disturbances and stress: A critical review. Bot. Mar. 52, 395–418. https://doi.org/10.1515/BOT.2009.057
– Boudouresque C.F., Bernard G., Bonhomme P., Charbonnel E., Diviacco G., Meinesz A., Pergent G., Pergent-Martini C., Ruitton S. & Tunesi L. (2012) Protection and conservation of Posidonia oceanica meadows. RAMOGE and RAC/SPA.
– Boudouresque C. F., Pergent G. & Pergent-Martini C., et al. (2015) The necromass of the Posidonia oceanica seagrass meadow: fate, role, ecosystem services and vulnerability. Hydrobiologia 781, 25–42. https://doi.org/10.1007/s10750-015-2333-y
– Boudouresque C.-F., Blanfuné A., Pergent G. & Thibaut T. (2021) Restoration of Seagrass Meadows in the Mediterranean Sea: A Critical Review of Effectiveness and Ethical Issues. Water, 13, 1034. https://doi.org/10.3390/w13081034
– Bruno M & Webster C. (2019) MedPAN et SPA/RAC. Le statut 2016 des aires marines protégées de Méditerranée. Ed SPA/RAC & MedPAN. Tunis, 222 pages.
– Bunuel X., Alcoverro T., Romero J., Arthur R., Ruiz J. M., Pérez M., Ontoria Y., Raventos N., Macpherson E., Torrado H. & Pagès J. F. (2020) Warming intensifies the interaction between the temperate seagrass Posidonia oceanica and its dominant fish herbivore Sarpa salpa. Marine Environmental Research, 165, 105237.
– Buonocore E., Donnarumma L., Appolloni L., Miccio A., Russo G. F. & Franzese P. P. (2020) Marine natural capital and ecosystem services: An environmental accounting model, Ecological Modelling, Vol 424, 109029, ISSN 0304-3800, https://doi.org/10.1016/j.ecolmodel.2020.109029.
– Bussotti S., Guidetti P. & Rossi F. (2022) Posidonia oceanica wrack beds as a fish habitat in the surf zone, Estuarine, Coastal and Shelf Science, Volume 272, 107882, ISSN 0272-7714, https://doi.org/10.1016/j.ecss.2022.107882.
– Campagne C. S., Salles J-M. Boissery P. & Deter J. (2015) The seagrass Posidonia oceanica: Ecosystem services identification and economic evaluation of goods and benefits. Mar. Pollut. Bull. http://dx.doi.org/10.1016/j.marpolbul.2015.05.061
– Carella F., Aceto S., Pollaro F., Miccio A., Iaria C., Carrasco N., Prado P. & De Vico G. (2019) A mycobacterial disease is associated with the silent mass mortality of the pen shell Pinna nobilis along the Tyrrhenian coastline of Italy. Sci Rep 9, 2725. https://doi.org/10.1038/s41598-018-37217-y
– Champenois W. & Borges A. V. (2012) Seasonal and interannual variations of community metabolism rates of a Posidonia oceanica seagrass meadow, Limnology and Oceanography, 57, doi: 10.4319/lo.2012.57.1.0347.
– Champenois W. & Borges A. V. (2019) Inter‐annual variations over a decade of primary production of the seagrass Posidonia oceanica. Limnol Oceanogr, 64: 32-45. https://doi.org/10.1002/lno.11017
– Coll M., Piroddi C., Albouy C., Ben Rais Lasram F., Cheung W.W.L., Christensen V., Karpouzi V.S., Guilhaumon F., Mouillot D., Paleczny M., Palomares M.L., Steenbeek J., Trujillo P., Watson R. & Pauly D. (2012) The Mediterranean Sea under siege: Spatial overlap between marine biodiversity, cumulative threats and marine 171 | P a g e reserves. Glob. Ecol. Biogeogr. 21, 465–480. https://doi.org/10.1111/j.1466- 8238.2011.00697.x
– Descamp P., Cornu T., Bougerol M., Boissery P., Ferlat C., Delaruelle G., Deter J. & Gobert S. (2017) Experimental transplantation of Posidonia oceanica. In Proceedings of the 13th International MEDCOAST Congress on Coastal and Marine Sciences, Engineering, Management and Conservation, Mellieha, Malta, 31 October–4 November 2017; Ozhan, E., Ed.; Mediterranean Coastal Foundation: Ortaca, Turkey.
– Deudero S., Morey G., Frau A., Moranta J. & Moreno I. (2008) Temporal trends of littoral fishes at deep Posidonia oceanica seagrass meadows in a temperate coastal zone, Journal of Marine Systems, Vol 70, Issues 1–2, Pages 182-195, ISSN 0924-7963, https://doi.org/10.1016/j.jmarsys.2007.05.001.
– Díaz-Almela E., Marbà N., Álvarez E., Santiago R., Holmer M., Grau A., Mirto S., Danovaro R., Petrou A. & Argyrou M. (2008) Benthic input rates predict seagrass (Posidonia oceanica) fish farm induced decline. Marine Pollution Bulletin 56 (7), 1332-1342. http://dx.doi.org/10.1016/j.marpolbul.2008.03.022.
– Duarte C.M. (2002) The future of seagrass meadows. Environ. Conserv. 29, 192–206. https://doi.org/10.1017/S0376892902000127
– Fernández Torquemada Y., González-Correa J. M., Mártinez J. E. & Sánchez-Lizaso J. L. (2005) Evaluation of the effects produced by the construction and expansion of marinas on Posidonia oceanica (L.) Delile meadows. J Coast Res 49: 94–99.
– Frederiksen M. S., Holmer M., Díaz-Almela E., Marba N. & Duarte C. M. (2007) Sulfide invasion in the seagrass Posidonia oceanica at Mediterranean fish farms: assessment using stable sulfur isotopes. Marine Ecology Progress Series 345, 93-104. http://dx.doi.org/10.3354/meps06990.
– Francour P. (1997) Fish Assemblages of Posidonia oceanica Beds at Port‐Cros (France, NW Mediterranean): Assessment of Composition and Long‐Term Fluctuations by Visual Census. Marine Ecology, 18: 157-173. https://doi.org/10.1111/j.1439-0485.1997.tb00434.x
– Francour P., Harmelin J. G., Pollard D. & Sartoretto S. (2001) A review of marine protected areas in the northwestern Mediterranean region: siting, usage, zonation and management. Aquatic Conservation: Marine and Freshwater Ecosystems 11, 155–188.
– Gacia E. & Duarte C. M. (2001) Sediment Retention by a Mediterranean Posidonia oceanica Meadow: The Balance between Deposition and Resuspension, Estuarine, Coastal and Shelf Science, Volume 52, Issue 4, 2001, Pages 505-514, ISSN 0272-7714, https://doi.org/10.1006/ecss.2000.0753.
– Gaylord B., Kroeker K.J., Sunday J.M., Anderson K.M., Barry J.P., Brown N.E., Connell S.D., Dupont S., Fabricius K.E., Hall-Spencer J.M., Klinger T., Milazzo M., Munday P.L., Russell B.D., Sanford E., Schreiber S.J., Thiyagarajan V., Vaughan M.L.H., Widdicombe S. & Harley C.D.G. (2015) Ocean acidification through the lens of ecological theory. Ecology 96, 3–15. https://doi.org/10.1890/14-0802.1
– Gobert S., Cambridge M. T., Velimirov B., Pergent G., Lepoint G., Bouquegneau J.-M., Dauby P., Pergent-Martini C. & Walker D. I. (2007) Biology of Posidonia. In: seagrasses: biology, ecologyand conservation. Springer, Dordrecht, pp 387-408, https://doi.org/10.1007/978-1-4020-2983-7_17
– González-Correa J. M., Sempere J. T. B., Sánchez-Jerez P., Valle C. (2007) Posidonia oceanica meadows are not declining globally. Analysis of population dynamics in marine protected areas of the Mediterranean Sea. Mar. Ecol. Prog. Ser. 2007, 336, 111–119.
– González-Correa J. M., Fernández-Torquemada Y. & Sánchez-Lizaso J. L. (2008) Long-term effect of beach replenishment on natural recovery of shallow Posidonia oceanica meadows. Estuarine, Coastal and Shelf Science, 76, 834-844.
– González-Correa J. M., Fernández-Torquemada Y. & Sánchez-Lizaso J. L. (2009) Short-term effect of beach replenishment on a shallow meadow. Marine Environmental Research, Elsevier, 68 (3), pp.143.
– Guala I., Simeone S., Buia M. C., Flagella S., Baroli M. & De Falco G. (2006) Posidonia oceanica ‘banquette’ removal: Environmental impact and management implications. Biol. Mar. Mediterr. 13: 149–153.
– Guerrero-Meseguer L., Sanz-Lázaro C. & Marín A. (2018) Understanding the sexual recruitment of one of the oldest and largest organisms on Earth, the seagrass Posidonia oceanica. PLoS One 13, e0207345. https://doi.org/10.1371/journal.pone.0207345
– Guerrero-Meseguer L., Marín A. & Sanz-Lázaro C. (2020) Heat wave intensity can vary the cumulative effects of multiple environmental stressors on Posidonia oceanica seedlings. Marine Environmental Research, 159, 105001.
– Guidetti P. (2000) Differences Among Fish Assemblages Associated with Nearshore Posidonia oceanica Seagrass Beds, Rocky–algal Reefs and Unvegetated Sand Habitats in the Adriatic Sea, Estuarine, Coastal and Shelf Science, Vol 50, Issue 4, Pages 515-529, ISSN 0272-7714, https://doi.org/10.1006/ecss.1999.0584.
– Hachani M. A., Ziadi B., Langar H., Sami D. A., Turki S. & Aleya L. (2016) The mapping of the Posidonia oceanica (L.) Delile barrier reef meadow in the southeastern Gulf of Tunis (Tunisia), Journal of African Earth Sciences, Volume 121, Pages 358-364, ISSN 1464-343X, https://doi.org/10.1016/j.jafrearsci.2016.05.030.
– Holmer M., Pérez M. & Duarte C. M. (2003) Benthic primary producers––a neglected environmental problem in Mediterranean maricultures? Marine Pollution Bulletin 46 (11), 1372-1376. http://dx.doi.org/10.1016/S0025-326X(03)00396-5.
– Holmer M., Argyrou M., Dalsgaard T., Danovaro R., Diaz-Almela E., Duarte C. M., Frederiksen M., Grau A., Karakassis I. & Marbà N. (2008) Effects of fish farm waste on Posidonia oceanica meadows: synthesis and provision of monitoring and management tools. Marine Pollution Bulletin 56 (9), 1618-1629. http://dx.doi.org/10.1016/j.marpolbul.2008.05.020.
– Houngnandan F. (2020) Impact des pressions anthropiques et de l’environnement sur les herbiers de Posidonia oceanica en Méditerranée française, Thèse en écologie biodiversité, Unité de recherche ISEM et MARBEC.
– Houngnandan F., Kéfi S. & Deter J. (2020) Identifying key-conservation areas for Posidonia oceanica seagrass beds, Biological Conservation, Volume 247, https://doi.org/10.1016/j.biocon.2020.108546.
– Hsü K., Montadert L., Bernoulli D., Bianca Cita M., Erickson A., Garrison R. E., Kidd R. B., Mèlierés F., Müller C. & Wright R. (1997) History of the Mediterranean salinity crisis. Nature 267, 399–403. https://doi.org/10.1038/267399a0
– Jackson E. L., Rees S. E., Wilding C. & Attrill, M.J. (2015) Use of a seagrass residency index to apportion commercial fishery landing values and recreation fisheries expenditure to seagrass habitat service. Conservation Biology, 29: 899 909. https://doi.org/10.1111/cobi.12436
– Kalogirou S., Corsini‐Foka M., Sioulas A., Wennhage H. & Pihl L. (2010) Diversity, structure and function of fish assemblages associated with Posidonia oceanica beds in an area of the eastern Mediterranean Sea and the role of non‐indigenous species. Journal of Fish Biology, 77: 2338-2357. https://doi.org/10.1111/j.1095-8649.2010.02817.x
– Katsanevakis S., Wallentinus I., Zenetos A., Leppäkoski E., Çinar M.E., Oztürk B., Grabowski M., Golani D. & Cardoso A.C. (2014) Impacts of invasive alien marine species on ecosystem services and biodiversity: A pan-European review. Aquat. Invasions 9, 391–423. https://doi.org/10.3391/ai.2014.9.4.01
– Kendrick G. A., Marbà N. & Duarte C. M. (2005) Modelling formation of complex topography by the seagrass Posidonia oceanica, Estuarine, Coastal and Shelf Science, Vol 65, Issue 4, Pages 717-725, ISSN 0272-7714, https://doi.org/10.1016/j.ecss.2005.07.007.
– Kletou D., Kleitou P., Savva I., Attrill M. J., Antoniou C. & Hall-Spencer J. M. (2018) Seagrass recovery after fish farm relocation in the eastern Mediterranean. Marine Environmental Research, doi: 10.1016/j.marenvres.2018.06.007.
– Koopmans D., Holtappels M., Chennu A., Weber M. & De Beer D. (2020) High net primary production of Mediterranean seagrass (Posidonia oceanica) meadows determined with aquatic eddy covariance, Front. Mar. Sci, Vol 7 : 118, doi : 10.3389/fmars.2020.00118
– Les D., Cleland M. & Waycott M. (1997) Phylogenetic Studies in Alismatidae, II: Evolution of Marine Angiosperms (Seagrasses) and Hydrophily. Systematic Botany, 22(3), 443-463. doi:10.2307/2419820
– Manca E., Cáceres I., Alsina J. M., Stratigaki V., Townend I. & Amos C.L. (2012) Wave energy and wave-induced flow reduction by full-scale model Posidonia oceanica seagrass, Continental Shelf Research, Volumes 50–51, Pages 100-116, ISSN 0278-4343, https://doi.org/10.1016/j.csr.2012.10.008.
– Marbà N. & Duarte C.M. (2010) Mediterranean warming triggers seagrass (Posidonia oceanica) shoot mortality. Glob. Chang. Biol. 16, 2366–2375. https://doi.org/10.1111/j.1365-2486.2009.02130.x
– Marbà N., Díaz-Almela E. & Duarte C. M. (2014) Mediterranean seagrass (Posidonia oceanica) loss between 1842 and 2009. Biol. Conserv. 176, 183–190. https://doi.org/10.1016/j.biocon.2014.05.024
– Martin A., Bernard G., Ize S. & Herlory O. (2018) Analyse économique de la gestion des plages : cas des banquettes de Posidonie sur les communes du littoral méditerranéen français. In: Paralia CFL (ed) XVèmes Journées Nationales Génie Côtier – Génie Civil. La Rochelle, France, p 683–692. doi: 10.5150/jngcgc.2018.079.
– Martin C.S., Giannoulaki M., De Leo F., Scardi M., Salomidi M., Knitweiss L., Pace M.L., Garofalo G., Gristina M., Ballesteros E., Bavestrello G., Belluscio A., Cebrian E., Gerakaris V., Pergent G., Pergent-Martini C., Schembri P.J., Terribile K., Rizzo L., Ben Souissi J., Bonacorsi M., Guarnieri G., Krzelj M., Macic V., Punzo E., Valavanis V. & Fraschetti S. (2014) Coralligenous and maërl habitats: Predictive modelling to identify their spatial distributions across the mediterranean sea. Sci. Rep. 4. https://doi.org/10.1038/srep05073
– Massa F., Onofri L. & Fezzardi D. (2017) Aquaculture in the Mediterranean and the Black Sea: a Blue Growth perspective. Paulo A.L.D., Lisa Emelia, S., Anil, M., (Eds.), Handbook on the economics and management of sustainable oceans. Edward Elgar- UnEnvironment. pp. 93-123.
– Mateo M. Á., Sánchez-Lizaso J. L. & Romero J. (2003) Posidonia oceanica ‘banquettes’: a preliminary assessment of the relevance for meadow carbon and nutrients budget, Estuarine, Coastal and Shelf Science, Volume 56, Issue 1, Pages 85-90, ISSN 0272-7714, https://doi.org/10.1016/S0272-7714(02)00123-3.
– Mateo M. Á., Cebrián J., Dunton K. & Mutchler T. (2006) Carbon flux in seagrass ecosystems. In: A.W.D. Larkum, R.J. Orth & C.M. Duarte (Eds), “Seagrass: Biology, Ecology and Conservation”, Springer Publ., New York: 157-191.
– Meinesz A., Cirik Ş., Akcali B., Javel F., Migliaccio M., Thibaut T., Yüksek A. & Procaccini G. (2009) Posidonia oceanica in the Marmara Sea, Aquatic Botany, Vol 90, Issue 1, Pages 18-22, ISSN 0304-3770, https://doi.org/10.1016/j.aquabot.2008.04.013.
– Milazzo M., Badalamenti F., Ceccherelli G. & Chemello R. (2004) Boat anchoring on Posidonia oceanica beds in a marine protected area (Italy, western Mediterranean): Effect of anchor types in different anchoring stages. J. Exp. Mar. Bio. Ecol. 299, 51–62. https://doi.org/10.1016/j.jembe.2003.09.003
– Mohr W., Lehnen N., Ahmerkamp S. et al. (2021) Terrestrial-type nitrogen-fixing symbiosis between seagrass and a marine bacterium. Nature 600, 105–109. https://doi.org/10.1038/s41586-021-04063-4
– Molenaar H. & Meinesz A. (1995) Vegetative Reproduction in Posidonia oceanica: Survival and Development of Transplanted Cuttings According to Different Spacings, Arrangements and Substrates. Botanica Marina, 38, 313-322
– Molenaar H., Meinesz A. & Thibaut T. (2009) Alterations of the Structure of Posidonia Oceanica Beds Due to the Introduced Alga Caulerpa Taxifolia. Scimar 2009, 73, 329-335.
– Montefalcone M., Albertelli G., Morri C., Parravicini V. & Bianchi C. N. (2009) Legal protection is not enough: Posidonia oceanica meadows in marine protected areas are not healthier than those in unprotected areas of the northwest Mediterranean Sea, Marine Pollution Bulletin, Volume 58, Issue 4, Pages 515-519, ISSN 0025-326X, https://doi.org/10.1016/j.marpolbul.2008.12.001.
– Occhipinti-Ambrogi A. (2007) Global change and marine communities: Alien species and climate change. Mar. Pollut. Bull. 55, 342–352. https://doi.org/10.1016/j.marpolbul.2006.11.014
– Pasqualini V., Clabaut P., Pergent G., Benyoussef L. & Pergent-Martini C. (2000) Contribution of side scan sonar to the management of Mediterranean littoral ecosystems. Int. J. Remote Sens. 21, 367–378.
– Pérez M., García T., Invers O. & Ruiz J.M. (2008) Physiological responses of the seagrass Posidonia oceanica as indicators of fish farm impact. Mar. Pollut. Bull. 56, 869–879. https://doi.org/10.1016/j.marpolbul.2008.02.001
– Pergent G., Bazairi H., Bianchi C. N., Boudouresque C. F., Buia M. C., Clabaut P., Harmelin-Vivien M., Mateo M. A., Montefalcone M., Morri C., Orfanidis S., Pergent-Martini C., Semroud R., Serrano O. & Verlaque M. (2012) Les herbiers de Magnoliophytes marines de Méditerranée : résilience et contribution à l’atténuation des changements climatiques. Gland, Suisse et Malaga, Espagne : IUCN. 80 pages.
– Pergent G., Bazairi H., Bianchi C.N., Boudouresque C., Buia M. & Calvo S. (2014) Climate change and Mediterranean seagrass meadows : a synopsis for environmental managers. Mediterr. Mar. Sci. Index. 462–473.
– Pergent-Martini C (1994) Impact d’un rejet d’eaux usées urbaines sur l’herbier à Posidonia oceanica, avant et après la mise en service d’une station d’épuration. PhD dissertation, University of Corsica.
– Pergent-Martini C., Leoni V., Pasqualini V., Ardizzone G. D., Balestri E., Bedini R., Belluscio A., Belsher T., J. Borg J., Boudouresque C. F., Boumaza S., Bouquegneau J. M., Buia M.C., Calvo S., Cebrian J., Charbonnel E., Cinelli F., Cossu A., Di Maida G., Dural B., Francour P., Gobert S., Lepoint G., Meinesz A., Molenaar H., Mansour H. M., Panayotidis P., Peirano A., Pergent G., Piazzi L., Pirrotta M., Relini G., Romero J., Sánchez-Lizaso J. L., Semroud R., Shembri P., Shili A., Tomasello A. & Velimirov B. (2005) Descriptors of Posidonia oceanica meadows: Use and application, Ecological Indicators, Volume 5, Issue 3, Pages 213-230, ISSN 1470-160X, https://doi.org/10.1016/j.ecolind.2005.02.004.
– Piazzi L., Acunto S., Frau F., Atzori F., Cinti M. F., Leone L. & Ceccherelli G. (2021) Environmental Engineering Techniques to Restore Degraded Posidonia oceanica Meadows. Water, 13, 661. https://doi.org/10.3390/w13050661
– Pirrotta M., Tomasello A., Scannavino A., Di Maida G., Luzzu F., Bellissimo G., Bellavia C., Costantini C., Orestano C., Sclafani G. & Calvo S (2015) Transplantation assesment of degraded Posidonia oceanica habitats : site selection and long-term monitoring. Medit. Mar. Sci., 16 (3) : 591-604.
– Randone M., Carlo G. & Di Costantini M., … T.T.-W.M.M., 2017, U., 2017. Reviving the Economy of the Mediterranean Sea: Actions for a Sustainable Future Rome: WWF.
– Ruiz J. M., Pérez M. & Romero J. (2001) Effects of fish farm loadings on seagrass (Posidonia oceanica) distribution, growth and photosynthesis. Marine Pollution Bulletin 42 (9), 749-760. http://dx.doi.org/10.1016/S0025-326X(00)00215-0
– Sánchez-Lizaso J. L., Fernandez Torquemada Y. & González-Correa J. M. (2009) Evaluation of the viability of Posidonia oceanica transplants associated with a marina expansion. Bot. Mar., 52, 471–476.
– Telesca L., Belluscio A., Criscoli A., Ardizzone G., Apostolaki E.T., Fraschetti S., Gristina M., Knittweis L., Martin C.S., Pergent G., Alagna A., Badalamenti F., Garofalo G., Gerakaris V., Louise Pace M., Pergent-Martini C. & Salomidi M. (2015) Seagrass meadows (Posidonia oceanica) distribution and trajectories of change [WWW Document]. Sci. Rep. https://doi.org/10.1038/srep12505
– Tomasello A., Di Maida G., Calvo S., Pirrotta M., Borra M. & Procaccini G. (2009) Seagrass meadows at the extreme of environmental tolerance: the case of Posidonia oceanica in a semi‐enclosed coastal lagoon. Marine Ecology, 30: 288 300. https://doi.org/10.1111/j.1439-0485.2009.00285.x
– Tomasello A., Pirrotta M.,& Calvo S. (2019) Construction underwater landscape by using Posidonia oceanica transplanting combined with innovative artificial reefs. In Proceedings of the 6th Mediterranean Symposium on Marine Vegetation, Antalya, Turkey, 14–18 January 2019; pp. 92–96.
– Vangeluwe D., Lepoint G., Bouquegneau J. M. & Gobert S. (2004) Effets de la transplantation sur les pousses de Posidonia oceanica. Vie et Milieu, 54 (4) : 223-230.
– Vassallo P., Paoli C., Rovere A., Montefalcone M., Morri C. & Bianchi C. N. (2013) The value of the seagrass Posidonia oceanica: A natural capital assessment, Marine Pollution Bulletin, Vol 75, Issues 1–2, Pages 157-167, ISSN 0025-326X, https://doi.org/10.1016/j.marpolbul.2013.07.044.
– Vázquez-Luis M., Álvarez E., Barrajón A., García-March J. R., Grau A., Hendriks I. E., Jiménez S., Kersting D., Moreno D., Pérez M., Ruiz J. M., Sánchez J., Villalba A. & Deudero S. (2017) S.O.S. Pinna nobilis: A Mass Mortality Event in Western Mediterranean Sea. Front. Mar. Sci. 4:220. doi: 10.3389/fmars.2017.00220
– Ward E. A., Meek S. K., Gordon D. M., Cameron T. C., Steer M. D., Smith D. J., Miliou A. & Tsimpidis T. (2020) The use of storm fragments and biodegradable replanting methods allows for a low-impact habitat restoration method of seagrass meadows, in the eastern Aegean Sea. Conservation Evidence, 17, 1-6.
– Williams S. L. (2001) Reduced genetic diversity in Z. marina transplantations affects both population growth and individual fitness. Ecol. Appl. 11 : 1472 – 1488
– Zunino S., Canu D. M., Marangon F. & Troiano S. (2020) Cultural ecosystem services provided by coralligenous assemblages and Posidonia oceanica in the Italian seas, Front. Mar. Sci. 6, 823. https://doi.org/10.3389/fmars.2019.00823
Ouvrage
Alexandre Meinesz & al. (2016) Méditerranée Mer Vivante, 19e édition, ed. Lions Clubs, 12-15p.
Sites Internet
– Boisleux Géraldine, Pean Michel, Harmelin Jean-Georges in : DORIS, 15/01/2021 : Posidonia oceanica (L.) Delile, https://doris.ffessm.fr/ref/specie/265
– Dossier Futura-Science écrit par le Pr. Charles-François Boudouresque : https://www.futura-sciences.com/planete/dossiers/nature-posidonie-miracle-mediterranee-2006/